总部位于新泽西州费尔菲尔德的Medimetriks Pharmaceuticals 宣布其合作伙伴Otsuka Pharmaceuticals UK在两项针对轻度至中度特应性皮炎的成年和儿科患者中MM36(地非拉司特)的两项III期临床试验中报告了阳性数据。研究在日本进行。
Difamilast是由Otsuka发现的新型特应性皮炎化合物stylechina.com。它抑制磷酸二酯酶4(PDE4)。这些类型的药物似乎通过抑制化学介质(如促炎性细胞因子和其他抗炎机制)的产生来改善特应性皮炎。
两家公司于2016年2月达成了许可协议。Medimetriks在美国和波多黎各拥有该药的独家开发和商业化权利以及制造权。根据交易条款,Medimetriks通过NDA批准向大冢支付了2200万美元的预付款和其他里程碑。Medimetriks在美国资助并处理了III期临床试验
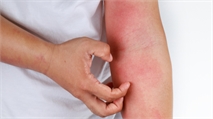
特应性皮炎是一种慢性炎症性皮肤病,会导致皮肤发红,肿胀和龟裂。发病最常发生在3到6个月大之间,约60%的患者在生命的第一年内发病,而90%的患者在5岁时发病。尽管有10%至30%的人一生都拥有它,但大多数人还是在儿童时期就解决了它。一小部分成年人会出现第一症状。在美国,约有1800万人患有特应性皮炎。当前的治疗包括局部皮质类固醇和局部钙调神经磷酸酶抑制剂。
“大冢公司今天宣布的结果令我们感到兴奋,并相信这些结果进一步证实了MM36(地非拉司特)作为轻度至中度特应性皮炎患者的最佳疗法的潜力,” 董事长兼首席执行官Bradley Glassman说。Medimetriks执行官。“我们正在为美国的III期MM36(二甲双胍)试验做准备,并致力于实现我们的目标,即帮助改善美国特应性皮炎患者的生活。”
两项临床试验是在日本进行的多中心,随机,双盲,载体对照,平行组研究。在成年人的研究中,患者每天两次接受1%的非米拉司软膏或安慰剂(载体)治疗,持续4周。在儿科研究中,还每天两次应用0.3%或1%的地非司特软膏或赋形剂,持续4周。使用研究者的全球评估(IGA)评估治疗效果,IGA是特应性皮炎临床试验的标准方法,该方法使用严重程度评分确定全身症状。
在两项试验中,IGA成功率的主要终点是活性药物治疗组中IGA评分为0(清晰)或1(几乎清晰)且至少改善了两个等级的患者比例更高与安慰剂组相比,差异具有统计学意义。没有观察到重大不良事件。
大冢表示计划进一步分析数据,并最终在科学会议上发布。
大冢公司同时还宣布,它与日本东京国立癌症中心共同开发了一项针对血液学癌症的综合基因组分析测试。它包括几乎所有类型的血液系统恶性肿瘤,包括急性髓细胞性白血病,骨髓增生异常综合症和骨髓增生性肿瘤,急性淋巴细胞白血病,淋巴瘤和骨髓瘤以及先天性骨髓衰竭综合征。该测定法将用于为患者和医生提供有关诊断,治疗和预后预测的详细信息。

